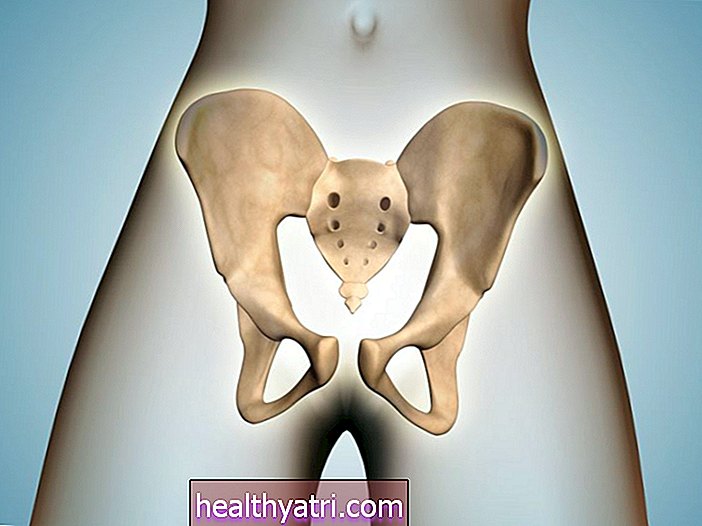
Antiretroviral terapi brukes til å behandle HIV og består av en kombinasjon av legemidler som blokkerer forskjellige stadier i virusets replikasjonssyklus. Ved å gjøre dette kan viruset undertrykkes til uoppdagelige nivåer der det kan skade kroppen lite.
Effektiviteten av kombinasjonen antiretroviral terapi ble først rapportert av forskere i 1996 på den internasjonale AIDS-konferansen i Vancouver, som kalt tilnærmingen HAART (svært aktiv antiretroviral terapi).
Justin Sullivan / Getty Images News / Getty ImagesI dag er begrepet HAART mindre brukt og har i stor grad blitt fortrengt i medisinsk litteratur av den forenklede ART (antiretroviral terapi). Endringen i terminologi handler om mer enn bare semantikk; det gjenspeiler et skifte i målene og fordelene med HIV-terapi og et skritt vekk fra det som HAART historisk antydet.
Før HAART
Da de første tilfellene av HIV ble identifisert i USA i 1982, skyndte forskerne seg for å finne måter å behandle et virus som hadde liten forrang i moderne medisin.
Det ville ta fem år før det første antiretrovirale legemidlet, kalt AZT (zidovudin), ble godkjent av US Food and Drug Administration (FDA) i mars 1987. Det ga publikum den første forsikringen om at sykdommen i stor grad ble ansett som en dødsdom, kan en dag bli kontrollert.
Til tross for det tidlige gjennombruddet, tilbød AZT bare beskjedne fordeler, og økte overlevelsestiden med i gjennomsnitt 24 måneder.
Den raske utviklingen av medikamentresistens gjorde at legemidlet ble brukt i økende grad, mens stoffets toksiske effekter ofte etterlot brukere med alvorlig anemi, leverproblemer og andre uutholdelige komplikasjoner.
I 1988 ble tre andre legemidler raskt godkjent - Hivid (ddC, zalcitabin), Videx (ddI, didanosin) og Zerit (d4T, stavudin) - og brukt i kombinasjonsterapier i et forsøk på å forlenge forventet levealder ytterligere. Og selv om de absolutt hjalp, viste de seg enda mer giftige enn AZT og krevde komplekse doseringsplaner, ofte med flere doser tatt hele dagen og natten.
Det forskerne raskt begynte å innse er at disse legemidlene - og de påfølgende som Viramune (nevirapin) og Epivir (3TC, lamivudin) - ikke oppnådde holdbar kontroll fordi de alle hadde lignende virkningsmekanismer og bare blokkerte ett av de syv stadiene i virusets replikeringssyklus.
Det ble foreslått at ved å målrette mot andre stadier, ville viruset ha langt mindre mulighet til å replikere og potensielt kunne bli fullstendig kontrollert. Dette løftet begynte å realiseres i 1995 med innføringen av en ny klasse antiretrovirale medisiner kjent som proteasehemmere (PI).
Fremkomst av HAART
I 1995 godkjente FDA den første proteasehemmeren kalt Invirase (saquinavir). I motsetning til andre antiretrovirale midler den gang, som blokkerte virusets evne til å "kapre" en celles genetiske maskineri og gjøre den om til en HIV-produserende fabrikk, PI blokkerte virusets evne til å samle nye kopier av seg selv fra strukturelle proteiner.
Denne en-to-tilnærmingen viste seg å være vendepunktet i den voksende pandemien.
Det ble rapportert på 1996-konferansen i Vancouver at strategisk bruk av tre legemidler fra hver av de to klassene var i stand til å oppnå og opprettholde en uoppdagelig virusbelastning, noe som effektivt satte sykdommen i remisjon.
Den nye tilnærmingen ble raskt kalt HAART og ble umiddelbart implementert som standard for pleie. I løpet av tre korte år falt HIV-dødsfall i USA og Europa med mer enn 50% - den første slike nedgangen siden pandemien startet.
Likevel var HAART langt fra perfekt, og den forventede levealderen, selv om den ble sterkt forbedret, var fortsatt mindre enn befolkningen generelt. Ved århundreskiftet kunne en 20-åring på antiretroviral terapi potensielt leve til begynnelsen av 50-årene.
Innenfor denne sammenhengen var "svært effektiv" like indikativ for HAARTs begrensninger som fordelene.
Utover HAART
Innen 2000 ble begrensningene for de tilgjengelige antiretrovirale medikamentene umiddelbart klare. Til tross for deres evne til å oppnå viral undertrykkelse, kan de være ekstremt utfordrende for brukeren av flere forskjellige grunner:
- Proteasehemmere fra den tiden var assosiert med potensielt alvorlige metabolske effekter, inkludert lipodystrofi (den noen ganger skjemmende omfordelingen av kroppsfett), insulinresistens og hjerterytmeforstyrrelser.
- AZT, Zerit og andre legemidler klassifisert som nukleosid revers transkriptasehemmere (NRTI) kan forårsake alvorlig perifer nevropati og potensielt livstruende melkesyreacidose.
- Legemidler fra tida var mindre "tilgivende" og utsatt for den raske utviklingen av medikamentresistens hvis behandlingsoverholdelse var noe mindre enn perfekt. Noen ikke-nukleosid revers transkriptasehemmere (NNRTI) som Viramune kunne utvikle resistens med bare en enkelt viral mutasjon .
- Noen proteasehemmere, som Invirase, krevde tre kapsler hver 8. time - en tidsplan som mange syntes det var vanskelig å opprettholde på lang sikt.
Så problematiske var disse problemene at HAART standard ble forsinket til immunfunksjonen falt under en viss terskel (nemlig et CD4-antall på mindre enn 350). Risikoen ved tidlig behandling på den tiden ble sett på å oppveie fordelene.
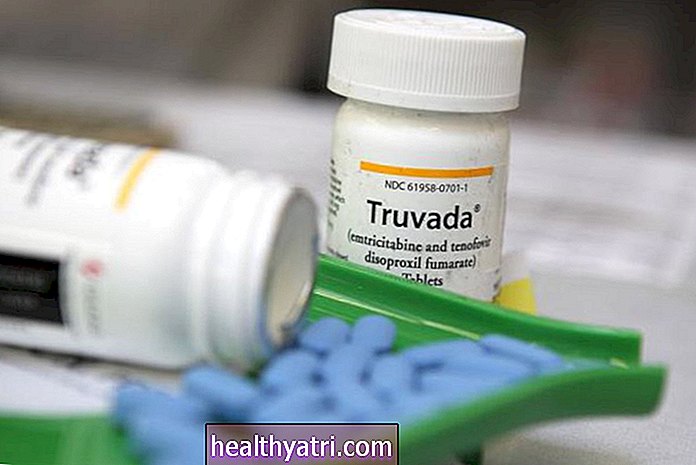
Alt dette endret seg i 2001 med introduksjonen av Viread (tenofovirdisoproksilfumarat), en ny type NRTI som hadde langt færre bivirkninger, kunne overvinne dyp motstand, og bare trengte en pille daglig.
Innen 2005, med forventet levealder og dødeligheten falt over hele verden, kunne forskere vise at behandlingen av HIV på tidspunktet for diagnosen forhindret alvorlig HIV-assosiert og ikke-HIV-assosiert sykdommer med forbløffende 61%.
Med universell behandling på diagnose som ble den nye standarden over hele verden, begynte det medisinske samfunnet å bruke ART for å beskrive en terapeutisk tilnærming som nå var mer enn bare "svært effektiv."
KUNST I dag
Hovedforskjellen mellom HAART på slutten av 1990-tallet / begynnelsen av 2000-tallet og ART i dag er at HIV virkelig kan betraktes som en kronisk, håndterbar tilstand. Ikke bare kan en 20-åring som er diagnostisert med HIV i dag, leve godt inn i 70-årene, men de kan gjøre det med medisiner som er tryggere, langvarige og lettere å ta.
Nyere medisiner og stoffklasser
De siste årene har nyere klasser av antiretrovirale legemidler blitt utviklet for å angripe viruset på forskjellige måter. Noen forhindrer tilknytning av HIV til vertsceller (inngangs- / vedleggshemmere), mens andre blokkerer integreringen av viral koding i vertscellens kjerne (integrasehemmere).
I tillegg er nyere versjoner av PI, NRTI og NNRTI blitt opprettet som gir bedre farmakokinetikk (legemiddelaktivitet), færre bivirkninger og bedre legemiddelresistensprofiler.
Et slikt eksempel er en oppdatert versjon av Viread kalt tenofovir alafenamid (TAF). I stedet for å levere legemidlet direkte, er TAF et inaktivt "prodrug" som omdannes av kroppen til tenofovir. Dette reduserer dosen fra 300 mg til 25 mg med samme kliniske resultater, samtidig som risikoen for nyreproblemer forbundet med bruk av Viread reduseres.
Kombinasjonsmedisiner med fast dose
En annen fremgang i terapi er utviklingen av faste dosekombinasjonsmedisiner (FDC) som kan levere komplett behandling med bare en pille daglig. I dag er det 13 av disse alt-i-ett-stoffene som er godkjent av FDA.
Enkeltpillerformuleringer forbedret ikke bare overholdelsesgraden, men har vist seg å redusere risikoen for alvorlige sykdommer og sykehusinnleggelser betydelig sammenlignet med antiretrovirale terapier med flere piller.
Omdefinere kombinasjonsterapi
Begrepet HAART har lenge vært synonymt med triple-drug therapy. Og selv om det er sant at ART vanligvis består av tre eller flere antiretrovirale midler, har forbedret farmakokinetikk nå gjort det mulig å behandle HIV med bare to antiretrovirale legemidler.
I 2019 godkjente FDA den første komplette to-legemiddelterapien kjent som Dovato, som kombinerer en nyere generasjons integrasehemmere kalt dolutegravir og en eldre NRTI kalt lamivudin. Kombinasjonen har vist seg å være like effektiv som standard trippelbehandling med færre bivirkninger.
Videre å snu definisjonen av ART på øret var frigjøringen av en injiserbar terapi kjent som Cabenuva i 2021.
Cabenuva er den førsteen gang i månedenterapi som er i stand til å oppnå vedvarende viral undertrykkelse med en injeksjon av integrasehemmeren cabotegravir og en injeksjon av en nyere NNRTI kalt rilpivirin.
Fremskritt som disse omdefinerer hva ART betyr og hva det til slutt kan bli.
Et ord fra veldig bra
Selv om målene for antiretroviral terapi forblir de samme, har ART i dag bare en tittende likhet med HAART fra fortiden. Uten unntak oppveier fordelene med behandlingen langt eventuelle bekymringer du har om medisinene eller deres bivirkninger.
Videre utvides fordelene til de som ikke er smittet. Landemerkeforskning publisert i en 2019-utgave avDeLancetkonkluderte med at mennesker med hiv som oppnår en uoppdagelig virus har null sjanse for å smitte andre.
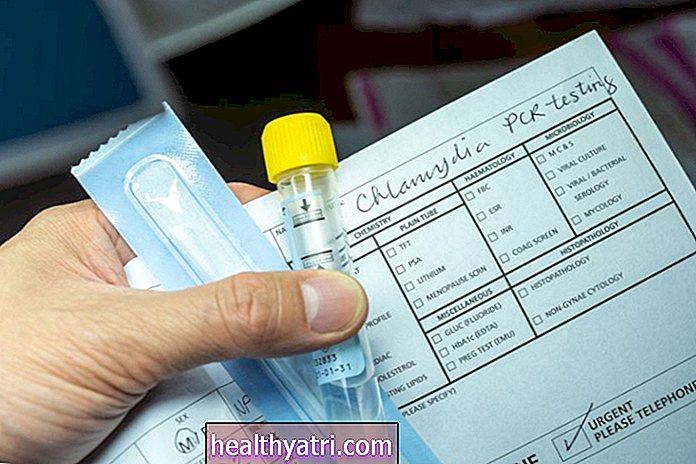
Disse faktorene peker videre på behovet for hiv-testing og illustrerer hvorfor U.S. Preventive Services Task Force anbefaler engangs hiv-testing av alle amerikanere i alderen 15 til 65 som en del av et rutinemessig legebesøk.











.jpg)