Roman coronavirus (COVID-19) har utviklet seg til en pandemi som har smittet millioner av mennesker over hele verden. Forskere og forskere jobber aktivt med å finne behandlinger for sykdommen, og ideelt sett finner de en måte å forhindre infeksjon i utgangspunktet.
Geber86 / Getty ImagesDet er hundrevis av kliniske studier på gang som evaluerer potensiell effektivitet av eksisterende medisiner, nye legemidler og tester levedyktigheten til vaksiner og blodprodukter. Følgende skisserer en liste over høyprofilerte behandlinger som er testet mot viruset, og starter med de som er i klinisk bruk for de som fortsatt er under utredning.
Per desember 2020 har ni behandlinger godkjenning i nødstilfelle fra US Food and Drug Administration (FDA), i rekkefølge av godkjenning: remdesivir (mai 2020), rekonvalesent plasma (august 2020), bamlanivimab monoklonalt antistoff (november 2020), kombinert baricitinib med remdesivir (november 2020), kombinerte casirivimab og imdevimab monoklonale antistoffer (november 2020), Pfizer-BioNTech mRNA-vaksinen (desember 2020), Moderna mRNA-vaksinen (desember 2020), kombinerte bamlanivimab og etesevimab monoklonale antistoffer (februar 2021), og Johnson & Johnson adenovirus-vektor-vaksinen (februar 2021).
Remdesivir
Remdesivir ble opprinnelig utviklet som en behandling mot ebola. Etter at in vitro-studier viste at det kan være effektivt mot COVID-19, fikk medfølende bruksanmodninger sykehus tilgang til legemidlet for behandling av alvorlig syke pasienter. 1. mai ble det det første behandlingsalternativet for COVID-19 å motta nødbrukstillatelse fra FDA. FDA har tillatt at den brukes hos voksne og barn innlagt på sykehus med alvorlige tilfeller av sykdommen. Den 22. oktober ble remdesivir det første legemidlet som ble godkjent av FDA for å behandle COVID-19 uten en nødbrukstillatelse. 19. november ble det også godkjent for et nytt EUA når det brukes i kombinasjon med baricitinib (se Biologics nedenfor).
Hva forskningen sier
En studie publisert iNew England Journal of Medicinesett på 61 tilfeller av medfølende bruk av remdesivir-behandling blant innlagte pasienter med COVID-19. Disse pasientene var alvorlig syke; ved studiestart var 30 på mekanisk ventilasjon og fire på ekstrakorporeal oksygenering av membran (ECMO). I løpet av et gjennomsnitt på 18 dager hadde 68% av pasientene forbedret oksygenering, og 57% av personene på ventilatorer var i stand til å bli ekstrubert. Imidlertid hadde så mange som 60% bivirkninger, og 23% av mennesker (alle i den mekaniske ventilasjonsgruppen) utviklet alvorlige komplikasjoner, inkludert syndrom med flere organer, septisk sjokk, akutt nyreskade og hypotensjon.
En klinisk studie - Adaptive COVID-19 Treatment Trial (ACTT) - av National Institutes of Health (NIH) - viste at personer med alvorlige COVID-19-infeksjoner som ble behandlet med stoffet, hadde forbedret symptomene 4 dager tidligere (31% raskere) enn de som ikke ble behandlet. Selv om det så ut til å være en forbedring i den totale overlevelsesraten, var dette ikke statistisk signifikant. Personer med moderate infeksjoner viste imidlertid ikke signifikant forbedring når de ble behandlet med 10 dagers remdesivir vs. standardpleie. Selv om det var forbedringer for personer som ble behandlet med 5 dager med remdesivir-behandling, bemerket forskerne at "forskjellen var av usikker klinisk betydning.
Data utgitt av legemiddelprodusenten Gilead Sciences bemerket forbedrede kliniske resultater i en randomisert kontrollstudie. Personer innlagt på sykehus med COVID-19 ble behandlet med remdesivir (n = 541) eller placebo (n = 521) i 10 dager. Mennesker i behandlingsgruppen kom seg fem dager raskere enn de i kontrollgruppen, trengte færre dager med oksygenstøtte og var mer sannsynlig å bli utskrevet tidligere.
I motsetning til dette fant Verdens helseorganisasjon (WHO) ingen klinisk fordel i deres solidaritetsforsøk. Denne studien inkluderte nesten 11 300 sykehusinnlagte med COVID-19 i 30 land. Studiedeltakere fikk en av fire behandlinger: hydroksyklorokin, interferon, lopinavir-ritanovir eller remdesivir. Ingen av behandlingene reduserte dødeligheten over 28 dager eller behovet for å starte ventilatorbehandling. Siden den gang har WHO formelt frarådet å bruke stoffet til sykehuspasienter. Gilead Sciences har utfordret disse resultatene, og en fagfellevurdering er på vent.
The National Institutes of Health anbefaler remdesivir, deksametason eller en kombinasjon av remdesivir med deksametason for pasienter som er innlagt på sykehus COVID-19 som trenger konvensjonell oksygenbehandling.
Dexametason og metylprednisolon
Dexamethason og methylprednisolone er steroider som ofte brukes til å behandle betennelse. De kommer i både muntlige og IV formuleringer. COVID-19 har i mange tilfeller vært assosiert med en alvorlig betennelsesreaksjon, og forskere så på å undersøke fordelene ved å bruke disse vanlige antiinflammatoriske legemidlene.
Hva forskningen sier
RECOVERY-studien (Randomized Evaluation of COVid-19 thERapY) -studien) har funnet at behandling med dexametason en gang daglig over 10 dager forbedret kliniske resultater sammenlignet med placebo. Spesielt reduserte dødeligheten fra 41% til 29% for pasienter som ble plassert i ventilatorer og fra 26% til 23% for personer som trenger oksygen uten ventilatorbehandling. Pasienter som ikke hadde behov for oksygen- eller ventilatorbehandling, så ikke klinisk fordel med deksametason.
En metaanalyse sponset av Verdens helseorganisasjon (WHO) gjennomgikk 7 randomiserte kliniske studier inkludert ca. 1700 kritisk syke COVID-19 pasienter. Publisert iJAMA, fant studien at dødeligheten på 28 dager var signifikant lavere for personer som ble behandlet med steroider (dexametason, hydrokortison eller metylprednisolon) enn for de som ble behandlet med vanlig pleie eller placebo (32% absolutt dødelighet for steroider mot 40% for kontroller) .
Steroider har vist fordeler når de brukes i kombinasjon med tocilizumab (se avsnittet Biologics nedenfor). En studie iAnnaler for revmatiske sykdommervurderte pasienter med COVID-19 som også hadde cytokin storm, et syndrom med overaktiv betennelse i kroppen. Pasienter som hadde COVID-19 og cytokin-storm ble behandlet med et høydose glukokortikoid, metylprednisolon, i fem dager. Hvis de ikke begynte å få klinisk bedring innen to dager, fikk de også en dose IV tocilizumab. Sammenlignet med personer behandlet med støttende pleie, var behandlingsgruppen 79% mer sannsynlig å ha klinisk forbedring i luftveissymptomer over 7 dager, 65% mindre sannsynlig å dø på sykehuset og 71% mindre sannsynlig å trenge mekanisk ventilasjon. Nok en studie, denne iBryst, bekreftet fordelen med å finne kombinasjonsbehandling hos 5776 pasienter innlagt på sykehus med COVID-19. Kortikosteroider reduserte dødeligheten med 34%, men dødeligheten falt med 56% når de ble kombinert med tocilizumab.
Barn som utvikler multisystem inflammatorisk syndrom hos barn (MIS-C) kan ha nytte av metylprednisolon, ifølge en studie iJAMA. I studien ble 111 barn med syndromet behandlet med IV-immunglobulin med eller uten metylprednisolon. Barn som fikk begge behandlingene hadde forbedret utfall, spesielt redusert feber innen 2 dager og redusert feberresidiv over 7 dager.
Kvaliserende plasma
Medisiner er en måte å målrette COVID-19 på, men våre egne kropper kan også tilby en måte å bekjempe sykdommen på. Når vi blir utsatt for et fremmed stoff som COVID-19, kan immunforsvaret vårt utvikle antistoffer mot det. Blod som inneholder disse antistoffene blir referert til som rekonvalesent plasma.
Å fjerne blodplasma fra noen som er syk og erstatte det med rekonvalesplasma fra noen som har kommet seg fra COVID-19, kan hjelpe dem med å bekjempe infeksjonen. Denne prosessen er kjent som plasmautveksling.
Hva forskningen sier
To små studier viste den potensielle fordelen med å bruke rekonvalesent plasma for behandling av alvorlige infeksjonstilfeller. En saksserie inkluderte fem pasienter med alvorlig lungebetennelse som trengte mekanisk ventilasjon. En egen pilotstudie inkluderte 10 pasienter med alvorlige COVID-19-infeksjoner. Alle pasienter gjennomgikk transfusjon med rekonvalesent plasma. Begge studiene bemerket forbedrede symptomer innen tre dager og redusert virusbelastning innen to uker (12 dager for case-serien, syv dager for pilotstudien). Evnen til å avvenne en ventilator var imidlertid langsom og oppnåddes ikke for alle pasienter. Viktigst, det så ut til at det ikke var noen skade forårsaket av behandlingen.
I april 2020 godkjente FDA to randomiserte, placebokontrollerte kliniske studier ved Johns Hopkins Medicine for å se om blodplasma kunne bidra til å forhindre COVID-19-infeksjon, ikke bare behandle de som er alvorlig smittet.
Resultatene har vært varierte. På en positiv note, en studie iMayo Clinic Proceedingsbemerket at ikke bare var rekonvalesent plasma generelt trygt når det ble brukt til å behandle 20 000 innlagte pasienter med COVID-19, det kan være forbundet med redusert dødelighet, spesielt når det ble gitt tidligere i løpet av sykdommen. Den hittil største studien behandlet mer enn 35.000 innlagte pasienter med rekonvalesent plasma. Resultatene antydet at behandling med plasma som hadde høye antistoffnivåer senket dødeligheten hvis den ble gitt innen 3 dager etter diagnosen. En studie av 160 COVID-19 pasienter fant behandling av eldre 65 år og eldre innen 3 dager etter milde symptomer reduserte risikoen for å utvikle seg til alvorlig luftveissykdom med halvparten (16% med behandling mot 31% med placebo) over 15 dager. Mens dødeligheten ikke ble vurdert i studien, anslår forskerne at bare syv eldre trenger å bli behandlet for å redusere alvorlig sykdom hos en voksen.
Ikke all forskning har vært like gunstig. En studie på nesten 500 voksne bemerket at mens rekonvalesent plasma reduserte virusbelastningen innen 7 dager, var det ingen reduksjon i dødeligheten. En randomisert kontrollert studie med 228 voksne med COVID-19 lungebetennelse fant ingen klinisk fordel for de som ble behandlet med rekonvalesjonsplasma i løpet av 30 dager. National Institutes of Health stoppet en klinisk studie i mars 2021 og noterte seg mangel på fordeler for personer med milde til moderate COVID-symptomer.
Uten mer konsistente eller robuste data har det vært kontroverser om FDAs beredskapstillatelse for rekonvalesent plasma som behandling for COVID-19 i august 2020. I februar 2020 ble EUA oppdatert. Bare høy-antistoff-titer-rekonvalesentplasma er nå godkjent for bruk. Det har også vært begrenset til sykehusinnlagte pasienter tidlig i løpet av sykdommen eller hos innlagte pasienter som er immunkompromitterte.
Konvalescent plasma kan samles opp som en bloddonasjon, og teknikker utføres for å sikre at plasmaet er fri for infeksjon. Det anbefales for øyeblikket at noen er symptomfrie i minst to uker før de donerer plasma.
Dusinvis av amerikanske sykehus er nå en del av National COVID-19 Convalescent Plasma Project, som jobber sammen for å undersøke terapeutisk plasmautveksling.
Regeneron Pharmaceuticals —Casirivimab og Imdevimab (tidligere REGN-COV2)
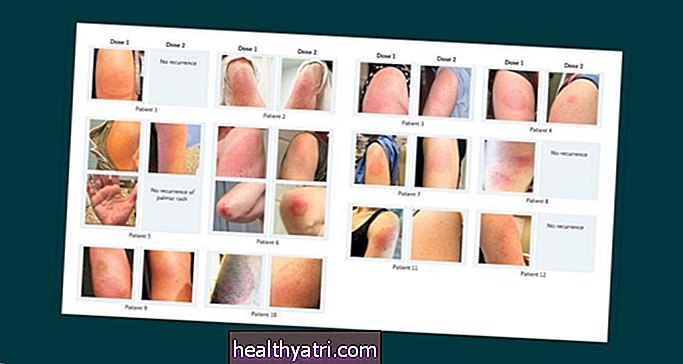
Regeneron Pharmaceuticals Inc. utviklet en menneskeskapt antibiotisk cocktail som opprinnelig ble kalt REGN-COV2, nå kjent som casirivimab og imdevimab. Undersøkelsesbehandlingen inkluderer to antistoffer rettet mot COVID-19. Selskapet kunngjorde foreløpige data som antydet at viral belastning og COVID-19 symptomer ble redusert innen 7 dager etter behandling. Etter å ha lagt til ytterligere 524 personer i studien, ble det funnet at REGN-COV2 reduserte behovet for COVID-relaterte medisinske besøk innen dag 29 sammenlignet med personer som ble behandlet med placebo (2,8% mot 6,8%). Forsøkene ble satt på vent for personer som krevde høytflytende oksygen eller mekanisk ventilasjon basert på "en ugunstig risiko / nytteprofil" i disse gruppene. President Donald Trump, som rapporterte positive COVID-19-testresultater 1. oktober, ble behandlet med REGN-COV2 2. oktober 2020.
21. november ga FDA godkjenning for nødbruk for antistoffcocktailen til personer med COVID-19 med mild til moderat sykdom som har høy risiko for komplikasjoner, som ikke er innlagt på sykehus og som ikke trenger ekstra oksygen. The National Institutes of Health sier imidlertid at denne behandlingen ikke skal være standard for pleie siden det er "utilstrekkelige data å anbefale enten for eller mot bruk av casirivimab pluss imdevimab for behandling av polikliniske pasienter med mild til moderat COVID-19".
Regeneron ga ut fase 3-forsøksresultater i en pressemelding og kunngjorde at deres casirivimab-imdevimab-cocktail reduserte COVID-19-infeksjonen hos personer med høyrisikoeksponering. Studien randomiserte 400 personer til behandling eller placebo. Personer som fikk cocktailen (n = 186) utviklet ikke symptomatiske infeksjoner, selv om 10 utviklet asymptomatiske infeksjoner. Placebogruppen (n = 223) utviklet imidlertid 8 symptomatiske infeksjoner og 23 asymptomatiske infeksjoner. Totalt sett reduserte behandlingen hastigheten på enhver COVID-19-infeksjon med halvparten (5% for behandlingsgruppen mot 10% for placebo) og fullstendig beskyttet mot symptomatisk infeksjon.
Andre syntetiske antistoffer
Regeneron Pharmaceuticals Inc. er ikke det eneste selskapet som ønsker å undersøke effektiviteten av syntetiske antistoffer laget i laboratoriet.
Eli Lilly - Bamlanivimab
Eli Lilly and Company er delvis sponset av National Institute of Allergy and Infectious Diseases, og har utviklet et monoklonalt antistoff (opprinnelig kjent som LY-CoV555, siden det heter bamlanivimab) som er ment å nøytralisere COVID-19. Fase 2 kliniske studier behandlet 452 personer med 3 doser hver. Selv om viral belastning ble redusert etter den andre dosen, hadde behandlings- og placebogruppene tilsvarende viral belastning etter den tredje dosen. Behandlingen reduserte imidlertid alvorlighetsgraden av symptomene fra dag 2 til 6 og reduserte antallet mennesker som ble værende på sykehuset på dag 29 (1,6% mot 6,3%). Forskning utviklet seg til fase 3 kliniske studier og kombinasjonsbehandling med remdesivir i ACTIV-3- studien. 13. oktober ble det imidlertid reist uspesifiserte sikkerhetsproblemer rundt behandlingen, og rettssaken ble satt på vent for innlagte pasienter.
9. november utstedte FDA en nødbrukstillatelse for denne behandlingen for høyrisikopersoner som har mild til moderat COVID-19, som ikke er innlagt på sykehus, og som ikke trenger oksygenbehandling på grunn av sin COVID-19-infeksjon.
I desember ble en studie av 314 personer med mild til moderat COVID-19 publisert iNew England Journal of Medicine. Alle deltakerne i studien ble behandlet med remdesivir, og eventuelt oksygen og / eller deksametason. De ble deretter randomisert til å motta bamlanivimab eller placebo. Forskerne bemerket at personer som ble behandlet med det nøytraliserende antistoffet ikke hadde forbedrede luftveissymptomer innen dag 5. Studien stoppet rekrutteringen på grunn av manglende effekt.
I en pressemelding rapporterte Eli Lilly om effektiviteten av bamlanivimab som en forebyggende behandling. I deres BLAZE-2-studie (resultatene er ennå ikke publisert) ble 965 sykehjemsbeboere som opprinnelig testet negativt for COVID-19, behandlet med det monoklonale antistoffet eller placebo. Over 8 uker var de som ble behandlet med bamlanivimab 57% mindre tilbøyelige til å utvikle symptomatisk COVID-19. Fire personer døde av infeksjonen, men ingen av dem var i behandlingsgruppen.
I februar 2020 ga FDA en nødbrukstillatelse for en kombinasjon av de monoklonale antistoffene bamlanivimab og etesevimab. Behandlingen er beregnet på pasienter som ikke er innlagt på sykehus med milde til moderate COVID-19 symptomer som ikke trenger ekstra oksygen. Pasienter bør være 12 år eller eldre, vekt minst 40 kg, og betraktes som høy risiko (f.eks. Være 65 år eller eldre, ha visse kroniske medisinske tilstander osv.). En randomisert, dobbeltblind, placebokontrollert klinisk studie med 1035 personer fant at de som fikk denne behandlingen, var mindre sannsynlig å bli innlagt eller dø av COVID-19 (2% mot 7%).
En fase 3-studie behandlet 769 COVID-19 pasienter med den monoklonale antistoffkombinasjonen eller placebo. Alle deltakerne var 12 år eller eldre, ble ansett som høyrisiko, hadde milde til moderate symptomer og ble ikke innlagt på sykehus ved studiestart. Fire personer i behandlingsgruppen krevde til slutt sykehusinnleggelse (4/511) mens 15 personer i placebogruppen var innlagt, hvorav 4 døde (15/258). Til sammen reduserte kombinasjonen bamlanivimab-etesevimab risikoen for sykehusinnleggelse eller død med 87%.
AstraZeneca - AZD7442
AstraZeneca vil starte fase 3 kliniske studier for å finne ut om antistoffer (AZD7442) kan behandle og forhåpentligvis forhindre COVID-19-infeksjon. Prekliniske studier viste effektivitet hos mus. Det brukes foreløpig ikke klinisk.
Vaksiner for COVID-19
Det beste håp for å håndtere COVID-19 langsiktig er å utvikle en vaksine. Vaksiner utsetter kroppen din for et antigen - et stoff som forårsaker en immunrespons, i dette tilfellet fra et virus - og utløser antistoffproduksjon fra immunforsvaret ditt. Målet er å lage antistoffer mot viruset uten å forårsake en infeksjon. På den måten, hvis du blir utsatt for det antigenet igjen, vil kroppen din huske hvordan du lager disse antistoffene mot det. Forhåpentligvis vil immunforsvaret være så sterkt at du ikke blir syk i det hele tatt. Men hvis du blir syk, vil symptomene dine være mildere enn om du ikke fikk vaksinen.
COVID-19 Vaksiner: Hold deg oppdatert om hvilke vaksiner som er tilgjengelige, hvem som kan få dem og hvor trygge de er.
Seks store vaksinekandidater har gjennomgått kliniske studier i USA.
Pfizer Inc. — Vaksinekandidat BNT162b2
Effekt: I november 2020 antydet tidlige data fra en fase III-studie at en mRNA-vektorert vaksine utviklet av Pfizer og BioNTech kan være 90% effektiv for å forhindre COVID-19. Vaksinen administreres i en to doseringsserie, med tre ukers mellomrom. Når vi så på infeksjonsrater 7 dager etter en andre dose, utviklet 94 personer symptomatisk COVID-19 fra en studiepopulasjon på 43 538 personer (30% var fargede). Dette satte vaksinen til mer enn 90% effekt. De ga ut ytterligere data 9 dager senere 18. november, og la merke til at 170 tilfeller av symptomatisk COVID-19 hadde forekommet hos deltakere, 8 tilfeller hos de som tok vaksinen og 162 hos personer som tok placebo. Dette forbedret dataene for å vise en 95% effektivitet generelt, en 94% effektivitet hos mennesker over 65 år. Etter å ha gjennomgått disse dataene, la FDA ut en briefing i desember som noterte seg en reduksjon i infeksjonsraten for vaksinerte studiedeltakere så tidlig som 10 til 14 dager etter deres første dose. Massevaksinering av nesten 600,00 mennesker i Israel har vist effektresultater som ligner på de i Pfizer kliniske studiene. Etter den andre dosen ble det bemerket at den var 92% effektiv mot COVID-19 generelt - 94% mot symptomatisk sykdom og 90% mot asymptomatisk sykdom. En preprint U.K. case control study så også på effektiviteten av vaksinasjon i den virkelige verden. Ser vi på omtrent 157000 eldre over 70 år, var en enkelt dose vaksine effektiv mot symptomatisk sykdom i hastigheter på 37% etter 14 dager, 55% etter 21 dager, 61% etter 28 dager og 57% etter 35 dager etter en enkelt dose. Etter en ny dose økte effektiviteten til 85 til 90%. Personer som utviklet symptomatisk COVID-19 etter den første dosen, var 43% mindre sannsynlig å kreve sykehusinnleggelse innen 14 dager etter diagnosen, og var 51% mindre sannsynlig å dø av infeksjonen.
Virusvarianter
Noen virusstammer, også kjent som varianter, har utviklet mutasjoner i piggproteinet som kan endre effektiviteten til noen vaksiner. Mange varianter har blitt oppdaget til dags dato. Her er tre av de mest undersøkte.
- Britisk variant: Også kjent som B.1.1.7 eller 20I / 501Y.V1, denne varianten inkluderer 17 mutasjoner (8 av dem i piggproteinet) og ble først oppdaget i september 2020.
- Sørafrikansk variant: Også kjent som B.1.351 eller 20H / 501Y.V2, denne varianten inkluderer 21 mutasjoner (10 av dem i piggproteinet) og ble først oppdaget i oktober 2020.
- Brasiliansk variant: Også kjent som B.1.28.1 eller 20J / 501Y.V3, denne varianten inkluderer 17 mutasjoner (3 av dem i piggproteinet) og ble først påvist i januar 2021.
Virusvarianter: Pfizer vurderte serumet til 40 personer som hadde mottatt begge dosene av vaksinen med 21 dagers mellomrom og testet det mot et virus som ligner på det opprinnelige viruset oppdaget i Wuhan, Kina (som en kontroll) og deretter mot et virus med spissen proteinmutasjoner funnet i den britiske varianten. Målet var å se hvor effektivt serumet var i å nøytralisere disse virusene. Serum fra yngre deltakere (23-55 år, n = 26) nøytraliserte den britiske varianten med 78% og de fra eldre deltakere (57-73 år, n = 14) med 83%. Deretter testet de mot andre varianter. Nøytraliserende antistoffanalyser ble utført på serumet til 20 vaksinerte personer ved bruk av et kontrollvirus, et virus med N501Y-mutasjonen for å representere de britiske og sørafrikanske variantene, 69/70-deletjon + N501Y + D614G-mutasjoner for å representere den britiske varianten, og virus med E484K + N501Y + D614G-mutasjoner for å representere den sørafrikanske varianten. I 6 av seraene var titrene bare halvparten så effektive mot den sørafrikanske varianten. Når det er sagt, i 10 av seraene var titrene dobbelt så høye mot den britiske varianten. Totalt forble vaksinen effektiv mot disse variantene, med en forskjell fra 0,81 til 1,46 ganger sammenlignet med kontrollen. En foreløpig rapport om serum fra 15 vaksinerte mottakere iNew England Journal of Medicinefant en to tredjedels nedsatt evne til å nøytralisere B.1.351-varianten. Pfizer ser på en tredje vaksinedose som en måte å øke antistoffresponsen mot COVID-19-varianter.
Barn: Pfizer undersøker effektiviteten av vaksinen deres hos barn. Fase III-studien inkluderer for tiden mer enn 2200 barn i alderen 12 til 15 og mer enn 750 ungdommer 16 til 17.
Lagring: Bekymringer har blitt reist om behovet for å lagre vaksinen ved hjelp av kaldkjedeteknologi, dvs. fryse den ved -70 grader Celsius (-94 grader Fahrenheit). Pfizer utviklet spesielle temperaturstyrte beholdere med tørris med GPS-termisk sporing for å sikre at vaksinen ble holdt ved riktig temperatur under forsendelse. Data levert til FDA har siden vist at vaksinen holder seg stabil ved standard frysetemperaturer opptil 2 uker. Dette vil forhåpentligvis gjøre vaksinen tilgjengelig på flere nettsteder.
Godkjenning: Vaksinen ble godkjent for bruk i Storbritannia 2. desember 8. desember 90 år gamle Margaret Keenan fra Storbritannia var den første ikke-studiedeltakeren i verden som fikk vaksinen. 11. desember ga FDA godkjenning for nødbruk i USA, og de første amerikanerne ble vaksinert 14. desember.
Kontrovers: Med økende spredning av COVID-19 kunngjorde Storbritannia planer om å administrere vaksinedoser med 12 ukers mellomrom i stedet for de anbefalte 3 ukene. Selv om dette vil øke antallet personer som får en første dose av vaksinen, har Pfizer og BioNTech uttalt at deres kliniske studier ikke har dataene som støtter effektiviteten av en slik doseringsplan. For øyeblikket vil USA fortsette med anbefalt doseringsplan for tre uker.
Moderna Inc. - Vaksinekandidat mRNA-1273
Foreløpige resultater: Finansiert av National Institute of Allergy and Infectious Diseases (NIAID) og Biomedical Advanced Research and Development Authority (BARDA), Moderna publiserte foreløpige resultater fra sin fase I-vaksineundersøkelse iNew England Journal of Medicinei juli 2020. Etter to doser av mRNA-vaksinen, administrert med 4 ukers mellomrom, utviklet de 45 studiedeltakerne nøytraliserende antistoffer i konsentrasjoner som var sammenlignbare med de som ble sett i rekonvalesent plasma. En påfølgende fase II-studie viste lovende resultater hos aper. Tjuefire rhesusmakaker ble behandlet med vaksine eller placebo og fikk to injeksjoner med 4 ukers mellomrom. De ble deretter direkte utsatt for høye doser COVID-19. Etter 2 dager hadde bare 1 av 8 av de vaksinerte apene detekterbart virus mens alle apene som ble behandlet med placebo hadde infeksjonen. Igjen var nøytraliserende aktivitet signifikant høyere enn den som ble sett med rekonvalesensserum. De oppdaget også en CD4 T-cellerespons mot piggproteinet.
Effekt: I november 2020 viste data fra fase III-studien at Moderna-vaksinen var 94,5% mot COVID-10. Når vi så på infeksjonsrater 2 uker etter en annen dose, utviklet 95 personer symptomatisk COVID-19 fra en studiepopulasjon på mer enn 30 000 mennesker som inkluderte mer enn 7 000 mennesker over 65 år og mer enn 11 000 mennesker i farger.Så mye som 42% av befolkningen hadde høyrisikoforhold som diabetes, hjertesykdom eller fedme. Av de som fikk sykdommen ble 11 tilfeller oppført som alvorlige, men ingen av dem hadde fått vaksinen. I desember ga de ut ytterligere data, og la merke til at 196 tilfeller av symptomatisk infeksjon hadde forekommet hos deltakere, 11 tilfeller hos de som tok vaksinen (ingen hadde alvorlig COVID-19) og 185 hos personer som tok placebo. Dette antydet 94,1% effekt for COVID-19 generelt og 100% effekt mot alvorlig sykdom. Peer-review av dataene venter.
Virusvarianter: Moderna utførte en in vitro-analyse og testet serumet fra 8 vaksinerte personer fra fase 1-studien mot variantene B.1.1.7 og B.1.351. Selskapet hevder at det ikke var noen signifikant reduksjon i nøytraliserende titere mot den britiske varianten, men bemerket en seks ganger reduksjon i titere til den sørafrikanske varianten. Av denne grunn undersøker de og utvikler en boosterdose for å målrette B.1.351-varianten. En foreløpig rapport om serum fra vaksinerte mottakere iNew England Journal of Medicinefant en marginal nedgang på 1,2 ganger i muligheten til å nøytralisere B.1.17-varianten, men en 6,4 ganger reduksjon i forhold til B.1.351-varianten.
Barn: Moderna fortsetter med prøvelser for barn helt ned til 12 år.
Varighet av immunitet: Det er viktig at Moderna også har publisert data om forventet varighet av vaksinresponsen. En fase I-studie vurderte 34 personer som mottok 2 doser av vaksinen med 28 dagers mellomrom, og sammenlignet antistoffresponsen med 41 kontroller som kom seg fra COVID-19. Forskerne fant at nøytraliserende antistoffer vedvarte 90 dager etter den andre dosen med vaksine og i høyere konsentrasjoner enn de som faktisk hadde sykdommen. Dette gir håp om at vaksinen kan tilby en rimelig periode med immunitet. Mer langsiktige data er nødvendig for å bestemme den sanne varigheten av immunresponsen.
Oppbevaring: I motsetning til Pfizer-vaksinen som krever kaldkjedeteknologi, kan Moderna-vaksinen oppbevares i standard frysere ved -4 grader Celsius (-20 grader Fahrenheit) i seks måneder, normale kjøleskapstemperaturer i 30 dager og romtemperatur i 12 timer.
Godkjenning: FDA ga Moderna-vaksine-nødbruksautorisasjon 18. desember 2020. De første dosene ble administrert 21. desember. Storbritannia godkjente denne vaksinen for bruk 8. januar 2021.
Kontrovers: FDA vurderer å redusere dosen av Moderna-vaksinen for å øke tilgjengelig tilbud og antall personer som kan vaksineres med en første dose. Data fra fase II-studier viser at halve doser av vaksinen ga samme nivå av immunitet som fulle doser for mennesker opp til 55 år. Imidlertid inkluderte dataene hundrevis av mennesker og kommer fra forsøk som tar sikte på å avgjøre om det var en immunrespons på vaksinen, dvs. utviklet antistoffer. Fase III-studiene var de som faktisk vurderte effektiviteten mot COVID-19. Full vaksinedose ble brukt i de sistnevnte studiene.
AstraZeneca - Vaksinekandidat AZD1222 (tidligere ChAdOx1)
Foreløpige resultater: I samarbeid med AstraZeneca har Oxford Universitys Jenner Institute steget fremover innen vaksineforskning. Fordi vaksinen mot en annen type coronavirus viste løfter i mindre forsøk på mennesker i fjor, var Jenner Institute i stand til å gå raskt fremover. Etter en første injeksjon av deres adenovirus-vektorerte vaksine, utviklet det seg nøytraliserende antistoffer hos 91% av de 35 studiedeltakerne som mottok vaksinen, nådde en topp på 28 dager og forble høy i 56 dager. Med en boostervaksine etter 4 uker ble det funnet nøytraliserende antistoffer hos alle deltakerne. Vaksinen deres hadde også en T-cellerespons som ble notert etter 7 dager, som toppet 14 dager og varte opptil 56 dager. Vaksinen midlertidigstoppet fase III-studien i september 2020 etter at en deltaker utviklet tverrgående myelitt, en nevrologisk tilstand som kan utløses av virus. Etter å ha bestemt at sykdommen ikke var forbundet med vaksinen, fortsatte AstraZeneca sin prøve etter 6 uker. I november ble flere fagfellevurderte fase II / III-data publisert. Med en økning til 560 studiedeltakere utviklet 99% av mennesker nøytraliserende antistoffer innen 2 uker etter boosterdosen.
Effekt: I desember publiserte AstraZeneca fagfellevurderte data på mer enn 11 000 deltakere på tvers av to forskjellige studieforsøk. Vaksineeffektiviteten var 62% etter at to fulldose-vaksiner ble administrert med en måneds mellomrom (n = 8 895) og 90% når de ble gitt en halv dose etterfulgt av en full dose en måned senere (n = 2741), for en kombinert effekt på 70,4%. I februar ga de ut flere fase III-data, denne gangen data om en større befolkning på mer enn 17 100 deltakere. Effekten etter en enkelt dose ble notert til å være 76% etter 22 til 90 dager (59% for full dose gruppen, 86% for halv dose gruppen). Effekt 14 dager etter to doser var 67% mot symptomatisk COVID-19 (57% for full dose gruppen, 74% for halv dose gruppen). Interessant nok ble effekten også påvirket av tidspunktet for dosene. Det var så lavt som 55% når dosene ble gitt mindre enn 6 ukers mellomrom (33% for full dose-gruppen, 67% for halvdose-gruppen), men økte til 82% når dosene ble skilt med minst 12 uker (63 % for full dose-gruppen, 92% for gruppen for halv dose). Merk at denne effekten er basert på at noen utvikler symptomer fra COVID-19 og ikke reflekterer asymptomatisk COVID-19-infeksjon. En forhåndsutskrevet case-control studie fra Storbritannia så på effektiviteten av enkeltdose vaksinasjon hos mennesker over 70 år. Forskerne så på omtrent 157 000 mennesker som ble testet for COVID-19 i den virkelige verden. Vaksineeffektivitet mot symptomatisk sykdom var 22% etter 14 dager, 45% etter 21 dager, 60% etter 28 dager og 73% etter 35 dager. Mennesker som utviklet symptomatisk COVID-19 til tross for vaksinering, var 37% mindre sannsynlig å kreve sykehusinnleggelse innen 14 dager etter diagnosen.
Virusvarianter: For å kontrollere effektiviteten mot B.1.1.7-varianten sekvenserte forskerne virusgenomet fra 499 fase II / III-deltakere som fikk COVID-19. Det var en 9 ganger reduksjon i nøytraliserende antistoffer mot B.1.1.7 sammenlignet med det opprinnelige viruset. For personer som ble utsatt for B.1.1.7-varianten, var effekten 75% mot symptomatisk COVID-19-infeksjon, men bare 27% mot asymptomatisk infeksjon. Dette var i kontrast til henholdsvis 84% og 75% for den opprinnelige stammen. Dessverre ble vaksineadministrasjonen stoppet i Sør-Afrika etter at data viste at den var ineffektiv mot mild til moderat COVID-19 forårsaket av B.1.351.
Lagring: I motsetning til mRNA-vaksinene, trenger ikke vaksinen å fryses ned og kan lagres ved normale kjøletemperaturer.
Godkjenning: Vaksinen ble godkjent for bruk i Storbritannia 30. desember 2020. De første dosene ble gitt 4. januar 2021. Verdens helseorganisasjon anbefalte bruk av vaksinen i februar 2020.
Kontrovers: I likhet med Pfizer-vaksinen, har Storbritannia kunngjort en endring av doseringsplanen for AstraZeneca-vaksinen fra 4 uker til 12 uker mellom dosene. Tilgjengelige data antyder at det er lignende effekt når den administreres med denne frekvensen for personer som fikk full dose av vaksinen.
Johnson & Johnson - Vaksinekandidat Ad26.COV2.S
Foreløpige resultater: Denne vaksinen er under utvikling av Janssen Pharmaceutical Companies, en avdeling av Johnson og Johnson. Det er en adenovirus-vektorert vaksine som angriper piggproteinet uttrykt av SARS-CoV-2. En studie på 52 rhesus macaque aper fant at en enkelt injeksjon utløste en nøytraliserende antistoffrespons med beskyttelse mot viruset. En fase I / II-studie med 56 voksne vurdert for sikkerhet ved bruk av en enkeltdose eller todoseplan. Etter en dose var serokonversjon (utvikling av antistoffer mot piggproteinet) 99% og T-celleresponsen mot piggproteinet nådde 83%. Vaksinen viser løfte da det er den eneste aktuelle kandidaten som vil kreve en enkelt dose i motsetning til to doser i serie. I oktober 2020 rapporterte Johnson & Johnson om en uforklarlig sykdom hos en av deltakerne i studien. Selskapet stoppet sin kliniske prøve i 11 dager til det ble forsikret om at sykdommen ikke var relatert til vaksinen. Siden den gang har flere fase I / II-data blitt publisert, som viser en nøytraliserende antistoffrespons i to forskjellige aldersgrupper i alderen 18 til 55 og 65 år og eldre. De sammenlignet også forskjellige doseringsregimer, for eksempel høy dose vs. lav dose og enkelt dose mot to doser med 56 dagers mellomrom. Til sammen ble 805 deltakere vaksinert. På dag 29 hadde gjennomsnittlig 90% av mennesker nøytraliserende antistoffer (92-99% for den yngre kohorten, 88-96% for den eldre kohorten, avhengig av doseringsregimet). På dag 57 var serokonversjon 100% for alle, uavhengig av alder eller doseringsregime.
Effekt: Deres fase 3-studie har inkludert mer enn 43.000 mennesker, og det har vært 468 tilfeller av symptomatisk COVID-19. Vaksinen var mest effektiv mot alvorlig infeksjon, og viste 85% effektivitet etter 28 dager uten tilfeller oppdaget etter dag 49. Effektiviteten samlet var 66%, (72% i USA, 66% i Latin-Amerika og 57% i Sør-Afrika ). Det bemerkes at 95% av tilfellene i Sør-Afrika var fra B.1.351-varianten.
Godkjenning: Johnson & Johnson-vaksinen ble godkjent av FDA som akutt bruk som en-dose vaksine 27. februar 2021. WHO ga autorisasjon 12. mars 2021.
Novavax Inc. - Vaksinekandidat NVX-CoV2373
Foreløpige resultater: Denne vaksinen, sponset av National Institute of Allergy and Infectious Diseases (NIAID) og Biomedical Advanced Research and Development Authority (BARDA), bruker nanopartikkelteknologi for å utvikle en antistoffrespons mot piggproteinet. Som mange av de andre vaksinene, administreres den i to doser med 21 dagers mellomrom. Fase I / II kliniske studier har vist en antistoffrespons som er større enn den som er sett i rekonvalesent plasma fra pasienter som var symptomatiske med COVID-19. En fase III-studie registrerer seg aktivt med sikte på 30 000 studiedeltakere, hvorav to tredjedeler vil motta vaksinen, resten placebo.
Effektivitet: I en pressemelding kunngjorde selskapet foreløpige resultater fra deres fase 3-prøve i Storbritannia (mer enn 15 000 deltakere) og deres fase 2-prøve i Sør-Afrika (mer enn 4400 deltakere). I den tidligere studien utviklet 62 deltakere symptomatisk COVID-19 (6 i behandlingsgruppen mot 56 i placebogruppen). Totalt var effektiviteten av vaksinen 89,3%. Dette brøt sammen til 95,6% mot den opprinnelige belastningen og 85,6% mot den britiske varianten. Sistnevnte studie var mindre vellykket, og bemerket 44 tilfeller av symptomatisk COVID-19 (15 i behandlingsgruppen mot 29 tilfeller i placebogruppen) med en samlet effektivitet på 60%. Sekvensering ble bare gjort på 27 av de positive tilfellene, men 25 av disse ble bekreftet å være den sørafrikanske varianten.
INOVIO Pharmaceuticals Inc. - Vaksinekandidat INO-4800
Coalition for Epidemic Preparedness Innovations og The Bill and Melinda Gates Foundation er blant de mange finansieringskildene for denne vaksinekandidaten. De første injeksjonene av denne DNA-vaksinen utviklet av INOVIO Pharmaceuticals, Inc. ble administrert til friske forsøkspersoner 6. april 2020. I september 2020 la FDA kliniske fase II / III-forsøk på vent mens den vurderer sikkerheten til leveringsanordningen injiserer DNA i celler. Selskapet forventer å gjenoppta forsøkene i andre kvartal 2021.
Biologics
Alvorlige tilfeller av COVID-19 har vært assosiert med det som kalles en cytokinstorm. Som en del av den normale immunresponsen rekrutterer kroppen cytokiner - proteiner utskilt av immunsystemceller - til infeksjonsstedet. I noen tilfeller blir imidlertid denne prosessen hyperresponsiv og overflødige cytokiner frigjøres. Noen av disse cytokinene er inflammatoriske og kan føre til forverring av luftveissymptomer eller organsvikt. Biologiske midler - farmasøytiske behandlinger opprettet fra biologiske kilder - vurderes nå å løse dette.
Baricitinib
Baricitinib er en JAK1 / JAK2-hemmer, en klasse medisiner som brukes mot betennelse ved å redusere effekten av visse cytokiner.
Hva forskningen sier: Som en del av Adaptive COVID-19 Treatment Trial (ACTT-2), har en fase III randomisert dobbeltblind placebokontrollert studie vist tidlig løfte for stoffet. Omtrent 1000 pasienter innlagt på sykehus med COVID-19 ble randomisert til å få remdesivir alene eller remdesivir med baricitinib. I gjennomsnitt forbedret pasientene seg klinisk en dag tidligere med kombinasjonsbehandlingen. I november 2020 godkjente FDA legemiddelkombinasjonen (ikke baricitinib alene) for en autorisasjonsbrukstillatelse for behandling av sykehusinnlagte pasienter som krevde oksygentilskudd, ventilatorbehandling eller ekstrakorporal membranoksygenering (ECMO). National Institutes of Health har imidlertid uttalt at det ikke er nok bevis for å støtte dette regimet som en foretrukket behandling når dexametason er tilgjengelig.
Interferon Beta-1a
Interferoner er en naturlig del av immunforsvaret ditt. Disse cytokinene øker immunresponsen mot virus. For tiden er interferoner for tiden en injisert behandling som brukes mot viral hepatitt.
Hva forskningen sier: Siden COVID-19 i de fleste tilfeller er en lungesykdom, så forskerne på om å puste interferon beta-1a i lungene kunne bidra til å øke immunresponsen mot viruset. En fase 2 randomisert dobbeltblindet klinisk studie iThe Lancet Respiratory Medicineså på omtrent 100 voksne innlagt på sykehus med COVID-19. Deltakerne ble behandlet med inhalert interferon beta-1a via forstøver eller placebo i 14 dager. Interferongruppen hadde to ganger den kliniske forbedringen etter 15 til 16 dager og tre ganger forbedringen på dag 28. Selv om lengden på sykehusoppholdet ikke ble redusert, var det en 79% reduksjon i alvorlighetsgraden av sykdom eller døende.
Tocilizumab
Tocilizumab er et monoklonalt antistoff som blokkerer cellereseptorer fra binding til interleukin-6 (IL-6), en av de proinflammatoriske cytokinene. Dette, i teorien, vil bidra til å redusere alvorlighetsgraden av cytokinstormen og hjelpe folk til å komme seg raskere.
Hva forskningen sier:
En studie iLancet revmatologifant 39% redusert risiko for bruk av ventilator eller død hos pasienter med COVID-19 lungebetennelse som ble behandlet med tocilizumab sammenlignet med de som ble behandlet med standardbehandling. Imidlertid fungerer tocilizumab som et immunsuppressivt middel, og forskerne fant også at de som ble behandlet med stoffet, også hadde en tredobling av utviklingen av andre nye infeksjoner som invasiv aspergillose. Ifølge en studie av 154 pasienter iKliniske smittsomme sykdommer, tocilizumab reduserte dødeligheten hos COVID-19 pasienter som trengte en ventilator med 45% sammenlignet med de som ikke ble behandlet med stoffet. Selv om de som ble behandlet med tociluzumab hadde større sannsynlighet for å utvikle superinfeksjoner (54% mot 26%) over en oppfølging på 47 dager, hadde de ikke økt død som følge av disse superinfeksjonene
Tre studier ble publisert iJAMA indremedisini oktober 2020, men resultatene var inkonsekvente. En amerikansk studie behandlet 433 personer med alvorlig COVID-19 innen to dager etter opptak på intensivavdeling. Dødeligheten deres var 29% sammenlignet med 41% for ICU-pasienter som ikke fikk tocilizumab. Franske og italienske studier fant imidlertid ingen klinisk fordel i sine randomiserte åpne forsøk for personer med COVID-19 lungebetennelse. Den tidligere studien så på 130 personer med moderat til alvorlig sykdom og sistnevnte på 126 personer. De fant ingen forskjell i dødeligheten ved henholdsvis 28 dager eller symptomforbedring ved behandling etter 14 dager. Nok en studie iNew England Journal of Medicineså på nesten 400 personer som hadde COVID-19 lungebetennelse. De som ble behandlet med tocilizumab hadde mindre sannsynlighet for å trenge mekanisk ventilasjon på dag 28 (12% mot 19% sammenlignet med standardpleie). Selv om kliniske resultater ble forbedret, endret ikke dødeligheten signifikant.
Dessverre har ikke alle studier vist fordeler. Noen har vist potensiell skade. En brasiliansk studie av 129 kritisk syke COVID-19 pasienter ble behandlet med tocilizumab med standardomsorg eller standardbehandling alene. Etter 15 dager var dødeligheten faktisk høyere for de som ble behandlet med tocilizumab, 17% mot 3%. Etter 29 dager var dødeligheten ikke statistisk signifikant mellom de to gruppene. Selv om andre studier har vist en overlevelsesfordel, reiser denne studien viktige spørsmål for sikkerhet. Faktisk ble denne studien avsluttet tidlig av den grunn.
National Institutes of Health anbefaler for tiden tocilizumab pluss deksametason for pasienter med COVID-19 i ICU som trenger mekanisk ventilasjon eller oksygen med høy strømning i nesekanylen. Ikke-ICU-pasienter som utvikler hypoksi og trenger ikke-invasiv ventilasjon eller oksygen med høy strømning, kan også kvalifisere for dette diettet, hvis de også har forhøyede inflammatoriske markører. Når det er sagt, bør ikke tocilizumab brukes til personer som er betydelig immunkompromitterte.
Andre antivirale midler
Det er en rekke antivirale behandlinger - medisiner som forhindrer virusets reproduksjonsevne - som blir undersøkt for COVID-19 på dette tidspunktet.
Molnupiravir
Molnupiravir er et medikament som blokkerer replikasjonen av noen RNA-virus. Det er et prodrug, et inaktivt medikament, som metaboliseres til sin aktive form (N4-hydroxycytidine) i kroppen. Legemidlet er utviklet av Merck og Ridgeback Biotherapeutics.
Hva forskningen sier: En fase 2-klinisk studie inkluderte 78 ikke-sykehusinnlagte personer med symptomatisk COVID-19 og påvisbare nivåer av virus på baseline nasofaryngeal vattpinne. Behandling med molnupiravir reduserte virusbelastningen til 0 innen dag 5 (0/47), men viruset kunne påvises hos 24% av placebogruppen (6/25). Ingen alvorlige bivirkninger ble tilskrevet behandlingen.
Influensamedisiner
Favipiravir og arbidol er antivirale medisiner som brukes til å behandle influensa. I høye konsentrasjoner kan de være effektive mot COVID-19.
Hva forskningen sier: I en studie av 240 pasienter med COVID-19 sammenlignet forskere favipiravirs effektivitet med arbidol. Symptomer på hoste og feber forbedret seg mye raskere med favipiravir enn med arbidol, men det var ingen signifikant forskjell i utvinningsgraden på dag syv. Begge medisinene ble godt tolerert med bare milde bivirkninger.
Lopinavir-Ritonavir
Lopinavir-ritonavir er et par antivirale medisiner som brukes til å behandle HIV som kan være effektive mot COVID-19.
Hva forskningen sier: I en studie på 199 personer med lungebetennelse fra COVID-19 og lave oksygenivåer, fikk 94 lopinavir-ritonavir og resten fikk placebo. Selv om flere mennesker behandlet med lopinavir-ritonavir hadde forbedret symptomene på dag 14 (45,5% mot 30%), var det ingen signifikant forskjell mellom de to gruppene når det gjaldt varigheten av oksygenbehandling, behovet for mekanisk ventilasjon, innleggelsestid eller dødelighet. En annen studie randomiserte 127 innlagte voksne med COVID-19 til enten trippelbehandling med lopinavir-ritonavir, ribavirin og interferon β-1b eller til lopinavir-ritonavir alene. Pasienter i gruppen med trippelterapi sluttet å kaste viruset tidligere (7 dager mot 12 dager), hadde tidligere forbedringer i symptomene (4 dager mot 8 dager) og forlot sykehuset tidligere (9 dager mot 15 dager).
Hydroksyklorokin og klorokin
Hydroksyklorokin og klorokin er medisiner som for tiden er FDA-godkjent for å behandle malaria og autoimmune sykdommer som lupus og revmatoid artritt.Ved å forstyrre proteinglykosylering og andre enzymatiske prosesser, antas det at disse medisinene kan forhindre COVID-19 i å binde seg til, komme inn og replikere i humane celler.
En studie som sammenligner hydroksyklorokin med klorokin fant at hydroksyklorokin er litt mindre potent, men likevel potensielt effektiv mot COVID-19 in vitro.
Hva forskningen sier
En fransk studie ledet an i hydroksyklorokin- og klorokinforskning. Den inkluderte opprinnelig 26 COVID-19 pasienter behandlet med et hydroksyklorokinregime og 16 ubehandlede kontrollpasienter. Seks av pasientene behandlet med hydroksyklorokin ble også behandlet med azitromycin (også kjent som en Z-Pack, som er foreskrevet for flere infeksjoner). På papiret så resultatene lovende ut. På dag seks bemerket studieforfatterne at personer som ble behandlet med hydroksyklorokin reduserte virusbelastningen - virusmengden i blodet - med 57%, og de som også ble behandlet med azitromycin hadde fjernet viruset helt.
Selv om dette var oppmuntrende, tok studien ikke opp hvordan pasientene klarte det klinisk, noe som betydde om symptomene deres begynte å bli bedre. Det var også uklart om behandlingen førte til de medisinske problemene som hindret deltakerne i studien fra å følge opp forskere (en døde, tre ble overført til intensivavdelingen, en stoppet behandlingen på grunn av bivirkninger av medisiner, en forlot sykehuset).
Mens FDA ga godkjenning for nødbruk for både klorokinfosfat og hydroksykloroksinsulfatprodukter for COVID-19 i mars, 15. juni, tilbakekalte den autorisasjonen, med henvisning til ineffektivitet og alvorlige bivirkninger.
Selv om det er anekdotisk bevis som støtter bruken av disse medisinene, har påfølgende studier ikke vist de samme fordelene. En annen fransk studie fulgte samme protokoll som den opprinnelige studien, men fant at hydroksyklorokin ikke forbedret symptomene betydelig eller reduserte klaring av viruset fra kroppen. Flere andre studier har vist at hydroksyklorokin ikke er mer effektivt enn placebo ved behandling av personer som hadde COVID-19. I september 2020, en dobbeltblind placebokontrollert randomisert klinisk studie iJAMA indremedisinkonkluderte med at hydroksyklorokin var ineffektivt i å forhindre smitte hos 132 helsepersonell. Det samme gjelder for folk som regelmessig tar hydroksyklorokin for å behandle revmatiske sykdommer. En annen studie viste at inntak av hydroksyklorokin ikke reduserte risikoen for å få COVID-19 sammenlignet med folk som ikke tok stoffet.
Mer om er de potensielle bivirkningene fra disse medisinene. En brasiliansk studie måtte avbrytes tidlig på grunn av komplikasjoner fra høye doser klorokin. ENJAMAstudien viste at behandling med hydroksyklorokin forlenget QT-intervallet hos mer enn 20% av pasientene med COVID-19, et funn på et elektrokardiogram (EKG) som kan være assosiert med utvikling av livstruende hjertearytmier.
Ikke alle rapporter er dårlige. Det er gitt ut en studie som viser potensielle fordeler for hydroksyklorokin ved behandling av COVID-19. Forskere studerte over 2500 voksne og fant at personer som ble behandlet med stoffet hadde en dødelighet på 14% sammenlignet med 26% uten det. Når hydroksyklorokin ble kombinert med azitromycin, var dødeligheten 20%. Det er imidlertid kontrovers over studien, fordi antall personer som ble behandlet med steroiddexametason var betydelig høyere i behandlingsgruppene, noe som tyder på at fordelen kan komme fra steroidet i stedet for hydroksyklorokin eller azitromycin. Mens 68% av alle deltakerne i studien ble behandlet med steroider, fikk bare 35% i gruppen som ikke var behandlet deksametason. Omtrent 79% i hydroksyklorokin-gruppen og 74% i den kombinerte hydroksyklorokin med azitromycin-gruppen hadde også fått steroider.
Et ord fra Verywell
Det er viktig å tilby håp i denne usikkerhetstiden, men det er også viktig at vi finner objektive, vitenskapelig beviste måter å beskytte oss på. Med hundrevis av kliniske studier på gang, må vi være på vakt når det gjelder å undersøke hva som fungerer og hva som ikke fungerer. Behandlinger må bevises trygge og effektive før vi bruker dem til å behandle store deler av befolkningen.