Melflufen (melphalan flufenamide) er et nytt legemiddel som undersøkes i behandlingen av tilbakefall eller ildfast myelomatose (RRMM). Det er et derivat av cellegiftet melphalan. Melflufen er et peptid-medikamentkonjugat; en kombinasjon av melfalan og et peptid (lite protein) bundet sammen. Melflufen gis ved intravenøs infusjon (i venen).
Legemidlet ble sendt inn som en ny legemiddelsøknad til US Food and Drug Administration (FDA) i juli 2020. FDA innvilget søknaden prioritert gjennomgang, og en avgjørelse forventes i slutten av februar 2021. Melflufen er ennå ikke allment tilgjengelig fordi det ikke er lisensiert og godkjent for bruk i myelom. Imidlertid kan pasienter behandles med legemidlet som en del av en klinisk studie.
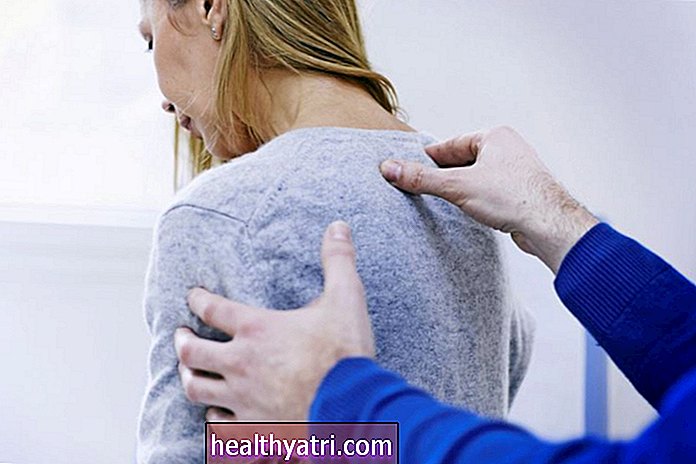
SimpleImages / Getty Images
Hva er multippel myelom?
Multipelt myelom er en type sjelden, uhelbredelig kreft i blodet, også kjent som hematologisk kreft. Det påvirker celler som kalles plasmaceller, som er typer hvite blodlegemer. Det finnes ingen kur mot myelomatose, og det kommer nesten alltid tilbake, på hvilket tidspunkt du sies å ha "tilbakefall eller ildfast" sykdom.
Hvordan fungerer Melflufen?
Etter hvert som nye kombinasjoner av anti-myelom medisiner blir introdusert i tidligere behandlingslinjer, har mennesker med RRMM ofte sykdom som er resistent mot flere legemidler.
Når Melflufen, kombinert med steroiddexametason, har potensial til å fylle dette medisinske behovet ved å tilby:
- En ny handlingsmekanisme
- Klinisk meningsfull effekt
- Håndterbar sikkerhet
Melflufen dreper myelomaceller ved bruk av peptidaser (enzymer som bryter ned peptider) som ofte finnes i høyere antall i myelomaceller enn i friske celler. Når melflufen kommer inn i myelomceller, bryter peptidasene i cellen bindingen som holder melphalan og peptidase sammen. Dette frigjør aktiv melfalan i myelomcellen. Melphalan forårsaker deretter irreversibel DNA-skade, noe som fører til celledød.
Hva forskningen sier
Forskning pågår for å finne nye behandlinger for myelomatose og finne måter å forbedre bruken av eksisterende.
For å hjelpe deg med forskning kan du bli bedt om å delta i en klinisk prøve under behandlingen.
Melflufen blir for tiden undersøkt som en behandling for RRMM-pasienter i kliniske studier. De kliniske studiene som har undersøkt effekten av melflufen inkluderer:
O-12-M1-studien
O-12-M1 var en internasjonal, multisenter, fase I / II-studie for å fastslå dosen av melflufen i kombinasjon med deksametason og undersøke behandlingsresponsen hos pasienter med RRMM, som var ildfaste (resistente) mot den siste behandlingslinjen. </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s> </s>
I O-12-M1-studien ble en gruppe på 45 pasienter som hadde fått minst to tidligere behandlinger registrert mellom juli 2013 og desember 2016. Studien forsøkte å oppdage den maksimalt tolererte dosen av melflufen. Den etablerte maksimale tolererte dosen var 40 mg melflufen i kombinasjon med deksametason.
Den høyeste dosen kohort testet (55 mg) overskred den maksimalt tolererte dosen fordi fire av seks pasienter opplevde alvorlige bivirkninger inkludert nøytropeni (lave hvite blodlegemer) og trombocytopeni (lavt antall blodplater); derfor ble den planlagte høyeste dosen på 70 mg ikke testet.
For forsøkspasientene førte behandling med melflufen og deksametason til sykdomsstabilisering hos 76% av pasientene.
Mediantiden til neste behandling - starten av behandlingen til neste behandling (eller til pasientens død, avhengig av hva som skjedde først) - var 7,9 måneder. Pasientene levde i en median på 20,7 måneder.
HORIZON klinisk prøve
I fase II HORIZON klinisk studie - som fant sted på 20 steder i hele USA og Europa - ble melflufen og dexametason gitt til totalt 154 pasienter som hadde fått et gjennomsnitt på fem tidligere behandlingslinjer.
Alle pasientene hadde tidligere blitt behandlet med et immunmodulerende legemiddel og proteasomhemmere, og de var resistente mot pomalidomid og / eller daratumumab.
Omtrent tre av ti pasienter (29%) svarte på behandlingen, og gjennomsnittlig tid før myelom begynte å komme tilbake var fire måneder. Disse resultatene indikerte at melflufen kan være gunstig for pasienter som tidligere har hatt flere behandlingslinjer.
Bivirkninger førte til reduksjon av doser av melflufen hos 27% av pasientene og doseforsinkelser hos 61% av pasientene. Den vanligste bivirkningen som førte til dosereduksjon var trombocytopeni (lavt antall blodplater), som forekom hos 14% av pasientene.
Alvorlige bivirkninger forekom hos 49% av pasientene generelt; vanligst rapportert var lungebetennelse (9%) og nøytropeni (5%). Andre primære maligniteter oppstod hos fem pasienter; av disse hadde fire maligniteter med kutane manifestasjoner. Totalt sett døde 10 pasienter (6%) av behandlingsrelaterte bivirkninger.
Dosering
Melflufen gis ved intravenøs infusjon (i venen). I kliniske studier har dosen vært:
- 40 mg melflufen den første dagen i hver behandlingssyklus
40 mg deksametason (redusert dose for pasienter 75 år eller eldre) på dag 1, 8, 15 og 22 i hver 28-dagers syklus
I noen studier ble dosen redusert hos de som opplevde en bivirkning.
Bivirkninger
De mest observerte bivirkningene av melflufen inkluderer:
• Lavt antall blodceller - nøytropeni og trombocytopeni
• Anemi
• Tretthet
• Infeksjoner, inkludert lungebetennelse og øvre luftveisinfeksjoner
• Kvalme og diaré
Fordi melflufen er et relativt nytt medikament, kan det oppstå nye bivirkninger som ennå ikke er rapportert.
Risiko
Ettersom forskning pågår, er det vanskelig å vurdere risikoen ved å ta melflufen for RRMM. Ettersom pasienter rekruttert til kliniske studier ofte har brukt opp tidligere behandlinger, er sjansene for bivirkninger eller til og med død under og etter behandlingen mulig.
Infeksjoner er en hovedårsak til sykelighet og dødelighet hos pasienter med RRMM, på grunn av et utarmet immunsystem. Det er viktig å regelmessig overvåke deg selv for tegn på infeksjon og rapportere eventuelle bekymringer til legen din så snart som mulig.


.jpg)