digicomphoto / Getty Images
Viktige takeaways
- Veklury (remdesivir) er den første FDA-godkjente behandlingen for personer med COVID-19.
- Godkjenningen er bare for behandling hos sykehuspasienter over 88 pund.
- Tidligere hadde legemidlet nødbrukstillatelse fra FDA.
Food and Drug Administration (FDA) godkjente Veklury (remdesivir) for behandling av COVID-19 hos sykehuspasienter 12 og eldre torsdag. Dette er det første offisielt FDA-godkjente medikamentet for COVID-19.
Tidligere hadde FDA gitt Emergency Use Authorization (EUA) for remdesivir, ikke full godkjenning. Den første EUA, utgitt 1. mai, sa at remdesivir kunne brukes på sykehuspasienter med alvorlig COVID-19. EUA ble gitt ut 28. august, og utvidet bruken til sykehusinnlagte voksne og barn med bekreftede eller mistenkte tilfeller COVID-19, uavhengig av sykdommens alvorlighetsgrad.
Selv om medikamentet nå er godkjent, omfatter ikke godkjenningen alle grupper. Pasienter må veie minst 40 kg (ca. 88 pund) for å få remdesivir. I et forsøk på å fortsette å tilby legemidlet til barn som dekkes av den første EUA når det er nødvendig, har FDA gitt ut på nytten annenEUA for remdesiver bruk i:
- Sykehusinnlagte pediatriske pasienter som veier 3,5 kg til mindre enn 40 kg
- Sykehusinnlagte pediatriske pasienter under 12 år som veier minst 3,5 kg
"FDA er forpliktet til å fremskynde utviklingen og tilgjengeligheten av COVID-19-behandlinger under denne enestående folkehelsesituasjonen," sa FDA-kommisjonær Stephen M. Hahn, MD i en uttalelse. "Dagens godkjenning støttes av data fra flere kliniske studier som byrået har vurdert grundig og representerer en viktig vitenskapelig milepæl i COVID-19-pandemien. Som en del av FDAs Coronavirus Treatment Acceleration Program, vil byrået fortsette å bidra til å flytte nye medisinske produkter til pasienter så snart som mulig, samtidig som det avgjøres om de er effektive og om fordelene deres oppveier risikoen.
Hva er Remdesivir?
Remdesivir er et direktevirkende antiviralt medikament som hemmer viral ribonukleinsyre (RNA) syntese. Coronavirus, inkludert SARS-CoV-2, er en familie av enkeltstrenget RNA-genom. Det er bevist at Remdesivir hindrer at disse virusene replikeres.
Remdesivir og COVID-19
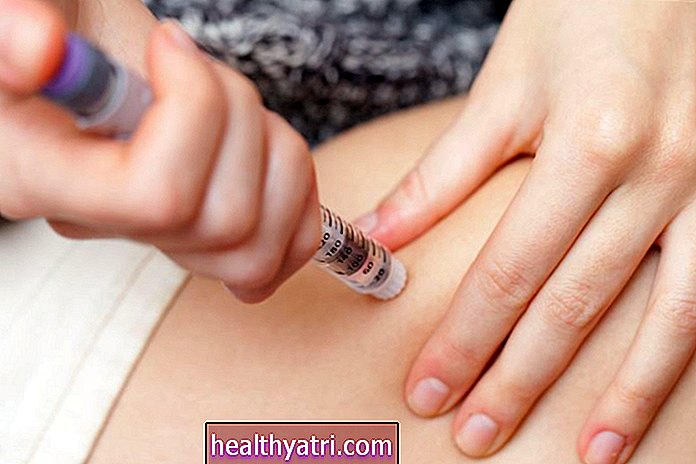
Remdesivir fikk først overskrifter på våren da Texas-forskere identifiserte det intravenøse medikamentet som "den mest lovende behandlingen" for COVID-19 til tross for begrensede kliniske data.
Da SARS-CoV-2 dukket opp, så forskerne lovende resultater etter å ha testet remdesivir på viruset i et laboratorium, og kliniske studier startet like etterpå, forklarer Matthew D. Hall, PhD, som jobber ved National Center for Advancing Translational Sciences at the National Institutt for helse. Han hjalp til med å lage COVID-19 OpenData Portal for å dele COVID-19-relaterte legemiddeldisponeringsdata og eksperimenter for alle godkjente medisiner.
”De fleste godkjente medisiner tar i gjennomsnitt 15 år og et par milliarder dollar å utvikle,” sier Hall til Verywell. ”Men vi hadde ikke 15 år; vi hadde ikke engang 15 uker. "
Hall sier at han og teamet hans hadde til oppgave å evaluere eksisterende ressurser.
"Vi trengte å se oss om etter de tingene som allerede var tilgjengelige for oss som enten var godkjent for å behandle andre sykdommer eller som ble utviklet for å behandle andre sykdommer," sier han. "De er kanskje ikke godkjent ennå, men forhåpentligvis har de vært hos mennesker, og vi vet at de er trygge. Vi er heldige nok til å ha mange antivirale legemidler. Av de legemidlene som er godkjent, eller legemiddelkandidater, ser remdesivir ut til å har vært den mest aktive, og det kan derfor flyttes til kliniske studier veldig raskt. "
Matthew D. Hall, PhD
De fleste godkjente medisiner tar i gjennomsnitt 15 år og et par milliarder dollar å utvikle. Men vi hadde ikke 15 år; vi hadde ikke engang 15 uker.
- Matthew D. Hall, PhDFDA innvilget opprinnelig en EUA 1. mai for å tillate sykehusinnlagte voksne pasienter med alvorlig COVID-19 å bli behandlet med remdesivir. En person med alvorlig COVID-19 ble definert som:
- En pasient med oksygenmetning mindre enn eller lik 94%
- En pasient som trenger ekstra oksygen
- En pasient som trenger mekanisk ventilasjon
- En pasient som trenger ekstrakorporeal oksygenering av membranen
Den utvidede EUA bidro til å gjøre legemidlet tilgjengelig for pasienter på tidligere stadier eller med mildere tilfeller av sykdommen, og godkjenningen skulle bare øke tilgjengeligheten. Hall sier at pasienter ikke trenger å bli registrert som en del av et klinisk spor for å få behandling, noe som øker tilgangen til mennesker som bor i landlige samfunn som ikke bor i nærheten av forskningsfasiliteter.
"Jeg tror at vi alle er enige om at det ville være bra for folk som bare er litt uvele hjemme, kan ta en antiviral medisin for å utrydde viruset fra kroppen deres for å sikre at de ikke blir sykere senere," sier Hall. "Akkurat nå må du vente til du er syk nok til å være på sykehus for å få remdesivir. Det ville være flott å sørge for at disse menneskene aldri er syke nok til å gå til sykehuset ved å gi dem en antiviral tidligere som Tamiflu for influensa, (hvor) du går til legen, får pillen og det vil forkorte tiden du er syk for. ”
Utvikling av Remdesivir
Remdesivir ble opprinnelig utviklet som en del av et samarbeid mellom Gilead Sciences, US Centers for Disease Control and Prevention og US Army Medical Research Institute of Infectious Diseases. Det ble utforsket som et potensielt terapeutisk middel under den vestafrikanske ebolavirusepidemien og for to andre koronavirus: alvorlig akutt respiratorisk syndrom (SARS) og Midtøsten respiratorisk syndrom (MERS).
Hvem bør ta Remdesivir?
Remdesivirs optimale pasientpopulasjon, dosering og behandlingsvarighet er ikke kjent. I et faktaark for helsepersonell tilbyr FDA følgende anbefalinger:
- For voksne og barn som veier 40 kg og mer, er anbefalt dose 200 mg på dag 1 etterfulgt av påfølgende doser på 100 mg.
- For pediatriske pasienter som veier mellom 3,5 kg og 40 kg, er anbefalt dose 5 mg / kg på dag 1 etterfulgt av påfølgende doser på 2,5 mg / kg.
- For pasienter som ikke trenger invasiv mekanisk ventilasjon og / eller ekstrakorporeal membranoksygenering, er den anbefalte totale behandlingsvarigheten 5 dager.
- For pasienter som trenger invasiv mekanisk ventilasjon og / eller oksygenering utenom kroppen, er den anbefalte totale behandlingsvarigheten 10 dager.
- Hvis en pasient ikke demonstrerer klinisk forbedring, kan behandlingen utvides i opptil 5 dager til i en total behandlingsvarighet på opptil 10 dager.
Gilead Sciences jobber med å skalere opp produksjon og distribusjon av remdesivir, som regnes som et undersøkelsesmedisin og for øyeblikket ikke er godkjent for noen indikasjon.
Kliniske studier og foreløpige funn
FDAs beslutning om å godkjenne remdesivir er basert på forskningsresultater fra noen få kliniske studier, og har blitt møtt med blandede meninger fra det medisinske samfunnet.
"Hva jeg synes om noe stoff eller en hvilken som helst medikamentkandidat, har ikke noe å si," sier Hall. “Det som virkelig betyr noe er data fra en velkontrollert klinisk studie. FDA ville ikke ha utvidet omfanget av EUA hvis de ikke trodde det ville være fordel for flere pasienter. "
I en studie publisert 29. april iThe Lancet,en gruppe leger og forskere gjennomførte en randomisert, dobbeltblind, placebokontrollert studie av 237 voksne pasienter med alvorlig COVID-19 på 10 sykehus i Hubei, Kina. De fant at remdesivir bidro til å øke utvinningen.
"Selv om det ikke var statistisk signifikant, hadde pasienter som fikk remdesivir en numerisk raskere tid til klinisk forbedring enn de som fikk placebo blant pasienter med symptomvarighet på 10 dager eller mindre," skriver forfatterne.
En amerikansk regjeringssponsert studie publiserte sine foreløpige funn 22. mai iNew England Journal of Medicinefra en randomisert, dobbeltblind placebokontrollert studie av 1063 COVID-19 pasienter. Forskere fant at de som fikk en 10-dagers løpet av remdesivir hadde kortere restitusjonstid sammenlignet med placebo - en median på 11 mot 15 dager.
"Disse foreløpige funnene støtter bruken av remdesivir for pasienter som er innlagt på sykehus med COVID-19 og krever supplerende oksygenbehandling," skriver forfatterne. "Gitt høy dødelighet til tross for bruk av remdesivir, er det imidlertid klart at behandling med et antiviralt medikament alene sannsynligvis ikke vil være tilstrekkelig."
21. august ble denTidsskrift for American Medical Associationpubliserte en randomisert fase-3-studie med 584 pasienter innlagt på sykehus med moderat COVID-19. lungebetennelse. Remdesivir-produsenten Gilead Sciences sponset denne studien på 105 sykehus i USA, Europa og Asia. Pasientene fikk enten en 5-dagers eller 10-dagers kur med remdesivir eller fikk standardbehandling. Forskere fant ingen forskjell i resultater blant 10-dagersgruppen, og liten meningsfull forskjell mellom 5-dagersgruppen.
Alle tre studiene møtte forskjellige begrensninger og hadde viktige forskjeller i design, så det er ikke rettferdig å lage en sammenligning av epler til epler. Imidlertid reiser det spørsmål om replikering av funn, et kjennetegn på klinisk forskning.
"Det er nå tre [randomiserte kontrollforsøk] av remdesivir hos innlagte pasienter med forskjellige resultater, og reiser spørsmålet om avvikene er gjenstander av valg av studiedesign, inkludert pasientpopulasjoner, eller om stoffet er mindre effektivt enn håpet," University of Pittsburgh School of Medicine forskere skrev i en lederartikkel publisert iTidsskrift for American Medical Association21. august. "Det virker derfor forsvarlig å raskt foreta ytterligere evalueringer av remdesivir i storstilt randomiserte kontrollforsøk som er utformet for å adressere den gjenværende usikkerheten og informere om optimal bruk."
Hva dette betyr for deg
U.S. Food and Drug Administration har gitt sin første COVID-19-behandlingsgodkjenning til remdesivir. Hvis du er innlagt på sykehus med et bekreftet eller mistenkt tilfelle av COVID-19, kan helsepersonell bestemme å forskrive dette legemidlet.
Hva er neste for Remdesivir?
Flere kliniske studier er i gang, ifølge nettstedet til Gilead Sciences. Selskapet er også i første fase av utviklingen for å formulere remdesivir som inhalator.
Hall sier at det globale samfunnet har kommet til utfordringen, men søket etter et medikament for SARS-CoV-2 har blitt forsterket av det faktum at det ikke finnes noen medisiner for menneskelige koronavirus. De siste utbruddene av SARS og MERS ble bekjempet gjennom folkehelsetiltak, ikke terapi.
"Med remdesivir er vi veldig heldige at det eksisterte," sier Hall. "Vi er heldige at det ble utviklet for ebola. Vi er heldige at det var tilgjengelig for å bli testet på mennesker nå. For hvis du trekker fra remdesivir fra ligningen, vet jeg ikke hva som er det nest beste. Det er ingen annet legemiddel godkjent for behandling av SARS-CoV-2-infeksjon. ”