Akutt myeloid (eller myelogen) leukemi (AML) undertype blir bedre forstått, med nye forskningsveier som blir utforsket. AML varierer sterkt fra person til person, og prognosen er ofte dårlig. Dette gjør forskning som kan bidra til å forbedre overlevelsesfrekvensen avgjørende.
Nye fremskritt de siste årene er å forbedre diagnostikk, behandlinger og overlevelsesrater, som alle gir et mer håpefullt syn.
AML er en kreft i blodet og benmargen (de svampete innsiden av bein der blodceller blir laget). Det er "akutt" fordi det utvikler seg raskt. "Myeloid" betyr at det involverer myeloide celler, som utvikler seg til forskjellige typer blodceller (f.eks. Røde og hvite blodlegemer, blodplater).
Albina Gavrilovic / Getty Images
Symptomer på AML inkluderer:
- Feber
- Bonesmerter
- Sløvhet og tretthet
- Hyppige infeksjoner
- Enkel blåmerke
- Uvanlig blødning
Undertyper vs. iscenesettelse
Når de fleste kreftformer blir diagnostisert, blir de "iscenesatt". Scenen forteller deg hvor avansert kreften er, bestemmer prognosen din og kan lede behandlingsbeslutninger.
AML er ikke iscenesatt. I stedet avhenger utsiktene og behandlingen av undertypen din, som bestemmes av laboratorietester.
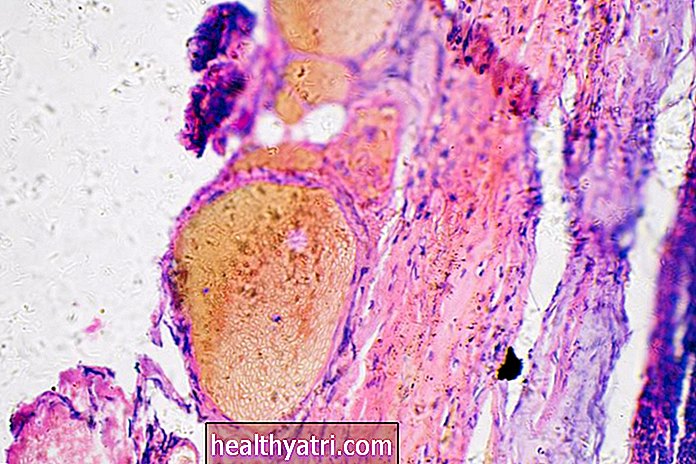
De fleste AML-undertyper er delvis definert av hvordan utviklede og unormale kreftceller ser ut under et mikroskop når sykdommen først diagnostiseres. I tillegg forsterkes AML-klassifiseringen nå av nye funn om genetiske endringer eller mutasjoner som er involvert.
To AML-klassifiseringssystemer er for tiden i bruk:
- Den fransk-amerikanske-britiske (FAB) klassifiseringen
- Verdens helseorganisasjon (WHO) klassifisering
Ytterligere klassifisering etter komplekse genetiske undertyper utvikler seg, takket være en banebrytende studie publisert i 2016.
Hvorfor undertype er viktig
Å vite den genetiske sammensetningen av leukemi kan hjelpe legen din med å forutsi om dagens behandlinger vil være effektive. Dette har allerede gjort mer omfattende genetisk testing på tidspunktet for diagnostiseringsrutinen.
Forståelse av undertyper kan også hjelpe forskere med å designe nye kliniske studier for å utvikle de beste behandlingene for hver AML-type.
Klassifisering av AML-undertyper
FAB-klassifiseringssystemet har eksistert siden 1970-tallet, men subtyping-prosessen har endret seg et par ganger de siste årene. WHO-klassifiseringssystemet ble standard i 2008, og grupperte mennesker basert på genetiske endringer som ligger til grunn for kreften deres (kalt "drivermutasjoner").
Så, i 2016, kom sentral forskning ut iNew England Journal of Medicine (NEJM)som har tatt undertyping enda lenger.
Denne studien viste at WHOs molekylære klassifiseringer ikke fungerer bra i nesten halvparten av AML-tilfeller - 48% av deltakerne i studien kunne ikke klassifiseres basert på WHOs molekylgrupper, selv om 96% av dem hadde drivermutasjoner.
Etterforskere har nå begynt å revurdere genomisk klassifisering av AML fra begynnelsen, basert på:
- Oppdagelsen av mange nye leukemi-gener
- Oppdagelsen av flere drivermutasjoner per pasient
- Komplekse mutasjonsmønstre
FAB Klassifisering av AML
For mer enn 40 år siden delte en gruppe franske, amerikanske og britiske leukemieksperter AML i undertyper M0 til M7 basert på hvilken type celle leukemi utvikler seg fra og hvor modne cellene er.
- M0 til M5 starter alle i umodne former for hvite blodlegemer.
- M6 starter i svært umodne former for røde blodlegemer.
- M7 starter i umodne former for celler som lager blodplater.
WHO Klassifisering av AML
FAB-klassifiseringssystemet brukes fortsatt ofte til å gruppere AML i undertyper; Imidlertid har kunnskapen avansert med hensyn til faktorer som påvirker prognose og utsikter for forskjellige typer AML.
Noen av disse fremskrittene ble reflektert i World Health Organization (WHO) -systemet i 2008, som deler AML i flere grupper:
- AML med myelodysplasi-relaterte endringer
- AML relatert til tidligere cellegift eller stråling
- Myeloid sarkom (også kjent som granulocytisk sarkom eller klorom)
- Myeloid spredning relatert til Downs syndrom
- AML med kromosomale translokasjoner og inversjoner
- AML ikke spesifisert
- Udifferensierte og bifenotypiske akutte leukemier
Gruppene 5, 6 og 7 er videre fordelt.
AML med kromosomale translokasjoner og inversjoner
I kromosomale translokasjoner bryter en del av det genetiske materialet fra sin opprinnelige plassering og festes på nytt til et annet kromosom. I inversjoner kommer et segment ut, vender opp ned og fester seg til det opprinnelige kromosomet.
Minst syv typer AML inkluderer translokasjoner, inversjoner eller lignende genetiske abnormiteter.
AML ikke ellers spesifisert
Tilfeller av AML som ikke faller inn i en av gruppene ovenfor er klassifisert på samme måte som FAB-systemet.
Udifferensierte og bifenotypiske akutte leukemier
Dette er leukemi som har både lymfocytiske og myeloide egenskaper. Noen ganger blir de kalt:
- Akutt lymfatisk leukemi (ALL) med myeloide markører
- AML med lymfoide markører
- Blandet akutt leukemi
Nye klassifiseringer: NEJM-studien
2016-studien som ba om nylig endring inkluderte 1.540 personer med AML. Forskere analyserte 111 gener som er kjent for å forårsake leukemi, med målet å identifisere "genetiske temaer" bak utviklingen av sykdommen.
De fant at deltakerne kunne deles inn i minst 11 hovedgrupper, hver med forskjellige klynger av genetiske endringer, og med forskjellige sykdomsegenskaper og funksjoner.
Ifølge studien hadde de fleste en unik kombinasjon av genetiske endringer som førte til leukemi, noe som kan bidra til å forklare hvorfor AML-overlevelsesraten varierer mye. Dermed jobbet forskerne med å utvikle et nytt AML-klassifiseringssystem ved hjelp av denne nye informasjonen.
De konkluderte med at det eksisterer tre undergrupper som ikke ble behandlet i WHO-klassifiseringssystemet. De kalles:
- Kromatin-spleisosom
- TP53-aneuploidi
- IDH2R172
Ved å bruke det foreslåtte systemet til å klassifisere de 1.540 studiedeltakerne:
- 1 236 personer med drivermutasjoner kunne hver klassifiseres i en enkelt undergruppe
- 56 pasienter oppfylte kriteriene for to eller flere undergrupper
- 166 personer med sjåførmutasjoner forble uklassifiserte
Forfatterne anbefalte at på kort sikt skulle fem spesifikke genetiske typer (kalt TP53, SRSF2, ASXL1, DNMT3A og IDH2) innlemmes i prognostiske retningslinjer fordi de er vanlige og sterkt påvirker resultatene.
Prognostic vs Diagnostic
NEJM-forskerne etterlyste to separate klassifiseringssystemer:
- En til bruk ved diagnostisering av mennesker
- En for bruk i å forutsi resultater (prognose)
De sier at diagnosesystemet bør være basert på faste egenskaper, mens det prognostiske systemet bør endres regelmessig basert på tilgjengelige behandlinger.
Nyere forskning
Basert i stor grad på NEJM-studien, har andre forskere undersøkt visse genetiske profiler av AML. I følge studier publisert i 2020 har noen forskere identifisert:
- Potensielle nye tidlige diagnostiske metoder for visse undertyper
- Potensielle nye måter å identifisere personer som sannsynligvis er medisinresistente
- Potensielle nye kombinasjoner av behandlinger for medikamentresistente tilfeller
En studie identifiserte et nytt medikament som forskere sier er effektivt mot medisinresistente AML-undertyper, og når det er i bruk, "vil det ha en umiddelbar klinisk innvirkning."
Diagnostisering av AML-undertyper
Leger har mange verktøy for å diagnostisere AML og bestemme undertypen din. Diagnosen starter med en fysisk eksamen. Under eksamen vil de se etter tegn som:
- Omfattende blåmerker
- Blør
- Infeksjon
- Avvik i øyne, munn, lever, milt eller lymfeknuter
For å bekrefte en mistenkt AML-diagnose, kan de bestille en hvilken som helst kombinasjon av følgende tester:
- Komplett blodtelling (CBC)
- Benmargsaspirasjon
- Benmargsbiopsi
- Lumbal punktering
- Bildebehandlingstester (f.eks. Røntgen, CT-skanning, MR)
- Cytogenetics
Cytogenetikk og molekylær testing er spesielt viktig for å bestemme undertypen din. Det innebærer å undersøke cellens genetiske materiale under et mikroskop for å lete etter genetiske abnormiteter, for eksempel translokasjoner og inversjoner.
Diagnostisering av leukemiUndertyper og AML-behandling
Et vell av nye AML-medisiner har blitt godkjent av Food and Drug Administration de siste årene; alle var imidlertid i utvikling i god tid før 2016-forskningen kom ut.
Nå, i stor grad basert på den forskningen, studeres for tiden mange potensielle behandlinger for AML basert på spesifikke genetiske undertyper.
Flere undersøkelsesmedisiner som er rettet mot visse genetiske mutasjoner har startet forskningsprosessen, og forskere ser også på nye typer cellegiftmedisiner, legemiddel- og antistoffkombinasjoner og legemidler som kalles kinasehemmere.
Noen av disse stoffene er allerede på markedet for andre forhold, mens andre viser lovende resultater i forsøk. For eksempel:
- Potensielle behandlinger for en AML-mutasjon kalt TET2 kan omfatte legemidler som kalles PARP-hemmere eller HMA kombinert med vitamin C.
- En gruppe enzymer kalt KAT kan hjelpe til med å behandle AML med mutasjoner i gener kalt EP300 og CBP.
- Legemidler som kalles p300-aktivatorer blir undersøkt i dyremodeller av AML.
Flere andre AML genetiske undertyper blir undersøkt slik at forskere kan finne ut hvilke medisiner som kan målrette dem.
Behandlingsalternativer for leukemiEt ord fra veldig bra
Akutt myeloid leukemi har alltid vært en skremmende diagnose med dårlig syn.
Men med nye medisiner tilgjengelig, mer på vei og stadig nye oppdagelser om genetiske undertyper, forbedrer prognosen og vil sannsynligvis fortsette å gjøre det.





.jpg)




.jpg)

.jpg)










.jpg)